Nem toda superfície que parece limpa está realmente livre de contaminação. Isso acontece por causa do biofilme, uma camada invisível de micro-organismos que se fixa nas superfícies e dificulta a remoção completa.
Em ambientes como hospitais, indústrias e áreas de manipulação de alimentos, isso exige mais cuidado. Controlar o biofilme depende de uma limpeza bem executada, com método, frequência adequada e uso correto dos produtos.
Biofilme: por que superfícies limpas ainda podem estar contaminadas?
A presença constante de micro-organismos em ambientes profissionais é um dos desafios mais complexos para as equipes de higienização. Mesmo quando os protocolos são seguidos corretamente, é comum que superfícies aparentemente limpas ainda apresentem contaminação. Um dos principais responsáveis por isso é o biofilme, que muitas vezes passa despercebido na rotina.
Essa formação é definida como uma comunidade estruturada de micro-organismos que se organiza sobre superfícies e desenvolve mecanismos de proteção contra agentes externos. Isso altera o comportamento microbiano e reduz a eficácia dos processos convencionais de limpeza e desinfecção.
Para dimensionar o problema, estudos indicam que a maioria dos micro-organismos não vive livre no ambiente, mas aderida a superfícies. Esse comportamento tem reflexos importantes na saúde humana, já que muitas infecções estão relacionadas à presença de biofilmes. Em hospitais, por exemplo, quando dispositivos médicos são colonizados, isso pode levar ao aumento do tempo de internação, necessidade de tratamentos adicionais e uso mais intenso de antimicrobianos.
Compreender o que são biofilmes, como se formam e por que resistem à higienização é, portanto, indispensável para qualquer profissional que atue no controle microbiológico, seja em hospitais, indústrias alimentícias, sistemas hidráulicos ou instalações de grande circulação.
Ao longo deste artigo, você vai entender como o biofilme se forma, por que ele resiste à limpeza, onde costuma aparecer com mais frequência, quais erros comprometem a higienização e quais práticas ajudam no controle e na prevenção. Tenha uma boa leitura!
O que é biofilme?
Biofilme é uma comunidade organizada de micro-organismos que se fixa em superfícies e forma uma camada protetora ao seu redor. Essa estrutura permite que bactérias, fungos e outros micro-organismos permaneçam ativos e mais resistentes, mesmo após processos de limpeza.
Historicamente, esses micro-organismos foram estudados como se vivessem livres no ambiente, dispersos em líquidos. Esse modelo influenciou diretamente a forma como pesquisas foram conduzidas e como produtos de limpeza e desinfecção foram desenvolvidos, incluindo a maioria dos testes de desempenho de desinfetantes.
Hoje se sabe que grande parte das bactérias, em condições naturais, vive aderida a superfícies e organizada em biofilmes. Esse entendimento avançou com o uso de tecnologias como a microscopia confocal, que permite visualizar micro-organismos em 3D sobre superfícies, e a biologia molecular, que analisa seu material genético e comportamento.
Dentro dessa estrutura, os micro-organismos produzem uma matriz protetora, conhecida como EPS (Extracellular Polymeric Substances), formada por açúcares complexos, proteínas, enzimas, DNA extracelular, lipídios e água.
Cada um desses componentes contribui para a resistência do biofilme. Os lipídios dificultam a entrada de soluções aquosas, o DNA ajuda a manter a estrutura estável e os exopolissacarídeos favorecem a fixação na superfície. O resultado é uma camada altamente protegida, capaz de resistir ao ressecamento, à radiação, à oxidação e até à ação de antibióticos e desinfetantes.
Isso muda a forma de encarar a limpeza profissional. Um desinfetante que apresenta bom desempenho em laboratório, onde as bactérias estão livres, pode ter um resultado muito menor quando essas mesmas bactérias estão organizadas em biofilme.
Por isso, é importante considerar que existem estruturas invisíveis a olho nu que continuam ativas mesmo após a limpeza. O controle do biofilme depende da combinação de ação mecânica, uso correto de produtos e processos bem definidos. É esse cuidado que diferencia uma limpeza apenas visual de um controle microbiológico mais consistente.
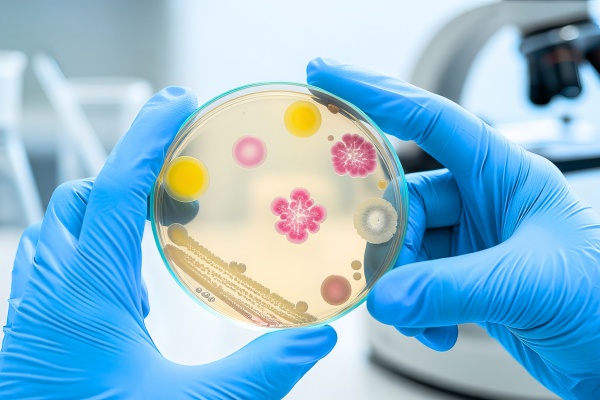
Bactérias em biofilme formam uma camada protetora difícil de remover
O que é biofilme bacteriano?
O biofilme bacteriano é uma das formas mais comuns e relevantes desse fenômeno em ambientes profissionais. Ele surge quando bactérias se fixam em uma superfície e começam a produzir uma camada protetora ao seu redor, que ajuda na fixação e dificulta sua remoção.
Algumas espécies têm maior impacto nesse cenário, especialmente em ambientes de saúde. Entre elas estão o Staphylococcus aureus, o Staphylococcus epidermidis e a Pseudomonas aeruginosa, frequentemente associadas a infecções mais graves, principalmente em pacientes com a imunidade comprometida.
Na indústria alimentícia, outras bactérias também merecem atenção, como a Listeria monocytogenes e a Salmonella spp., conhecidas por formar estruturas resistentes em superfícies de preparo e processamento de alimentos.
Um ponto que chama atenção é a forma como essas bactérias se organizam. Elas “se comunicam” entre si por meio de sinais químicos, em um processo chamado quorum sensing. De forma simples, isso permite que elas “percebam” quando há um número suficiente de células e, a partir disso, iniciem juntas a formação da camada protetora e ativem mecanismos de defesa.
Ou seja, não é algo aleatório. Trata-se de um processo organizado, que torna o biofilme muito mais resistente e difícil de remover do que bactérias que estão livres no ambiente. É justamente por isso que métodos tradicionais de limpeza nem sempre conseguem resolver o problema por completo. Desinfetantes de alto desempenho podem contribuir para uma maior eficácia na higienização de superfícies sujeitas à formação de biofilme bacteriano.
+SAIBA MAIS: Desinfetante Hospitalar Optigerm Oxikill Pronto Uso
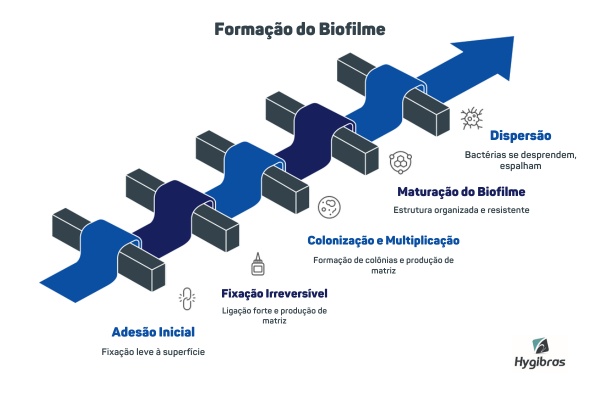
Como são formados os biofilmes?
O biofilme não surge de uma vez. Ele se forma aos poucos, passando por etapas bem definidas. Entender esse processo ajuda a identificar o melhor momento para agir e também explica por que, depois de certo ponto, a remoção se torna mais difícil.
Veja abaixo como esse processo acontece.
1. Adesão inicial (reversível)
Tudo começa quando bactérias livres entram em contato com uma superfície e se fixam de forma ainda leve. Nessa fase, elas podem se desprender com facilidade. Condições como umidade, presença de resíduos orgânicos e características da superfície facilitam essa aproximação.
2. Fixação irreversível
Com o tempo, essa ligação se fortalece. As bactérias passam a produzir estruturas e substâncias que garantem uma fixação mais estável, tornando difícil a remoção com ações simples, como enxágue ou limpeza superficial. A partir desse ponto, elas começam a se multiplicar e a atrair outras células, dando início à formação de uma estrutura mais complexa.
3. Colonização e multiplicação
Após se fixarem, as bactérias se multiplicam rapidamente e formam pequenas colônias. É nessa fase que começa a produção da matriz que sustenta o biofilme. Essa estrutura retém água, nutrientes e micro-organismos, criando um ambiente protegido e favorável ao crescimento. Ao mesmo tempo, as bactérias passam a se organizar de forma coletiva, o que acelera o desenvolvimento do biofilme.
4. Maturação do biofilme
Nessa fase, o biofilme já está completamente estruturado e mais resistente. Ele forma uma espécie de rede organizada, com canais internos que distribuem nutrientes, água e oxigênio, além de eliminar resíduos. Essa organização permite que os micro-organismos continuem ativos mesmo em condições menos favoráveis, o que dificulta ainda mais sua remoção.
5. Dispersão
Na etapa final, parte das bactérias se desprende dessa estrutura e volta ao estado livre. Essas células podem se fixar em outras superfícies e iniciar um novo ciclo. Por isso, sem controle adequado, o biofilme tende a se espalhar de forma contínua dentro do ambiente.
Por que o biofilme é resistente à limpeza?
A resistência do biofilme à higienização é um dos pontos que mais chamam atenção, e também um dos que mais geram dúvidas. O que dificulta o controle não é um único fator, mas a combinação de várias características que se reforçam ao mesmo tempo.
Matriz protetora e dificuldade de penetração dos desinfetantes
A matriz que envolve o biofilme funciona como uma barreira. Ela dificulta a entrada dos desinfetantes, principalmente nas camadas mais internas. Além disso, alguns componentes dessa estrutura podem reagir com os produtos químicos e reduzir sua ação antes mesmo de atingirem as bactérias.
Por isso, um desinfetante que apresenta ótimo desempenho em laboratório pode ter sua eficácia bastante reduzida quando aplicado sobre um biofilme já formado. Bactérias organizadas dessa forma conseguem suportar condições muito mais agressivas do que aquelas que estão livres no ambiente.
Metabolismo reduzido das células internas
Nas regiões mais profundas do biofilme, as bactérias entram em um estado de baixa atividade conhecido na literatura como “células persisters“. Elas continuam vivas, mas com metabolismo reduzido. Esse estado é temporário, e essas células voltam a se desenvolver quando encontram condições favoráveis.
O desafio é que muitos desinfetantes atuam justamente em processos ativos da célula. Quando essa atividade está reduzida, o efeito do produto diminui. Isso ajuda a explicar por que certas contaminações persistem mesmo após várias tentativas de tratamento.
Estrutura interna não uniforme
O biofilme não é igual em toda a sua extensão. Dentro dele, existem áreas com diferentes níveis de oxigênio, nutrientes e pH. Isso cria regiões com comportamentos distintos dentro da mesma estrutura.
Na prática, isso significa que um mesmo produto pode agir em uma parte do biofilme, mas não em outra. Enquanto as bactérias da superfície podem ser afetadas, as mais protegidas continuam ativas, mantendo a estrutura viva.
Produção de enzimas protetoras
Algumas bactérias presentes no biofilme produzem enzimas capazes de neutralizar agentes químicos. Essas substâncias se espalham pela matriz e acabam protegendo não apenas quem as produziu, mas toda a comunidade ao redor.
Esse tipo de defesa coletiva se fortalece conforme o biofilme se desenvolve, aumentando ainda mais a dificuldade de controle.
Transferência de genes de resistência
Dentro do biofilme, as bactérias ficam muito próximas umas das outras. Isso facilita a troca de material genético, incluindo genes ligados à resistência a antimicrobianos.
Com o tempo, essa troca torna a comunidade mais preparada para resistir aos produtos utilizados. Quando produtos são aplicados em concentrações abaixo do recomendado, esse efeito pode se intensificar, favorecendo a sobrevivência das bactérias mais resistentes.
Onde os biofilmes podem surgir nos ambientes profissionais?
O biofilme pode se formar em qualquer superfície que reúna três condições básicas: umidade, presença de matéria orgânica e tempo suficiente para que os micro-organismos se fixem.
Essas condições são mais comuns do que parecem e estão presentes em diferentes tipos de ambientes profissionais, muitas vezes sem qualquer sinal visível. Por isso, identificar os pontos mais críticos em cada setor ajuda a direcionar melhor os esforços de controle.
Ambientes hospitalares
Nos hospitais, superfícies de contato frequente, como grades de leito, mesas de procedimento, monitores e equipamentos de apoio, estão constantemente expostas a micro-organismos.
Dispositivos médicos invasivos, como cateteres, endoscópios, próteses e implantes, aumentam ainda mais esse risco, já que entram em contato direto com fluidos e tecidos do paciente. A ANVISA reconhece o biofilme como um fator relevante nesse cenário e reforça a necessidade de protocolos rigorosos de limpeza e desinfecção.
A presença de biofilme em ambientes hospitalares está associada ao aumento das infecções relacionadas à assistência à saúde (IRAS), ao prolongamento do tempo de internação, ao uso mais intenso de antimicrobianos e ao aumento dos custos hospitalares.
Outro ponto importante é que muitos testes laboratoriais são feitos com bactérias livres, e não organizados em biofilme. Isso pode gerar uma percepção de eficácia maior do que a observada na prática clínica, onde essas estruturas estão presentes.
Indústria alimentícia
Na indústria de alimentos, o biofilme representa um risco constante para a segurança dos produtos. Equipamentos, utensílios, esteiras e superfícies de preparo são pontos críticos, principalmente quando há resíduos orgânicos que não foram totalmente removidos.
Estudos com Salmonella spp. mostram que a resistência do biofilme pode variar de acordo com o tipo de material da superfície, o que reforça a necessidade de adaptar os protocolos de limpeza para cada situação.
Além dos riscos à saúde do consumidor, a presença de biofilme pode levar a não conformidades, recalls e prejuízos à imagem da empresa. A ANVISA, por meio da RDC nº 216/2004, exige que os processos de higienização em serviços de alimentação sejam bem definidos, com especificação de produtos, métodos, frequência, concentração e tempo de contato.
Ambientes industriais
Em ambientes industriais, o biofilme não afeta apenas a questão microbiológica. Ele também pode danificar equipamentos. Isso acontece porque alguns micro-organismos produzem substâncias que aceleram a corrosão de superfícies metálicas, um processo conhecido como biocorrosão.
Com o tempo, isso compromete a estrutura dos equipamentos, reduz sua vida útil e aumenta os custos de manutenção. Em setores como o petroquímico e o alimentício, esse problema também pode afetar a qualidade dos produtos e a segurança das operações.
Sistemas hidráulicos e tubulações
Tubulações e sistemas de distribuição de água são pontos críticos para o desenvolvimento de biofilme. A combinação de fluxo constante, temperatura e presença de matéria orgânica cria um ambiente ideal para a proliferação de micro-organismos. Ao mesmo tempo, a dificuldade de acesso torna a limpeza mais complexa.
Um caso preocupante é a presença de Legionella pneumophila, bactéria que pode se desenvolver nesses sistemas e causar a doença dos legionários, uma forma grave de pneumonia.
Além disso, o biofilme nesses sistemas favorece a troca de características de resistência entre bactérias, tornando tubulações e reservatórios verdadeiros focos de disseminação. Por isso, o monitoramento desses pontos vai além da manutenção e passa a ser uma questão de saúde pública.
Ambientes corporativos e áreas de grande circulação
Espaços como escritórios, shoppings e aeroportos também apresentam condições favoráveis para a formação de biofilme, embora muitas vezes isso não receba a devida atenção.
Superfícies de alto contato, como corrimãos, maçanetas, teclados e mesas, acumulam micro-organismos ao longo do dia. Quando a limpeza não é feita de forma adequada ou com a frequência necessária, esse acúmulo pode evoluir para a formação de biofilme e facilitar a contaminação entre as pessoas que utilizam o espaço.
| Ambiente | Onde o biofilme se forma | Principais riscos |
| Hospitalar | Superfícies de contato frequente e dispositivos médicos | Aumento de infecções (IRAS), prolongamento de internações e maior uso de antimicrobianos |
| Indústria alimentícia | Equipamentos, utensílios, esteiras e áreas de preparo | Contaminação de alimentos, não conformidades, recalls e prejuízos à imagem da empresa |
| Industrial | Superfícies metálicas e equipamentos | Biocorrosão, redução da vida útil dos equipamentos e aumento dos custos de manutenção |
| Sistemas hidráulicos | Tubulações, reservatórios e sistemas de água | Proliferação de bactérias como Legionella e riscos à saúde pública |
| Áreas de circulação | Corrimãos, maçanetas, teclados e mesas | Acúmulo de micro-organismos e maior risco de contaminação cruzada entre pessoas |
Tabela mostrando onde os biofilmes podem surgir
Casos de hantavírus e a importância da higiene preventiva nos ambientes
Nos últimos meses, os casos de hantavírus divulgados pela mídia voltaram a chamar a atenção para os riscos da contaminação ambiental em locais com acúmulo de sujeira, poeira, resíduos orgânicos e presença de roedores. O hantavírus é um vírus transmitido principalmente pelo contato com partículas contaminadas presentes na urina, fezes e secreções de roedores infectados.
A transmissão costuma ocorrer quando esses resíduos secam no ambiente e pequenas partículas contaminadas são dispersas no ar durante movimentações, limpezas inadequadas ou circulação em locais fechados e sem ventilação adequada.
Ambientes como depósitos, galpões, estoques, áreas pouco utilizadas, forros, cozinhas industriais, lixeiras, tubulações, ralos e locais com falhas de conservação podem favorecer o acúmulo de matéria orgânica e criar condições propícias para contaminações ambientais.
Embora o biofilme e o hantavírus sejam temas diferentes, ambos reforçam um ponto importante dentro da higienização profissional: muitos riscos biológicos não são visíveis a olho nu e podem permanecer presentes mesmo em superfícies aparentemente limpas.
No caso do biofilme, micro-organismos conseguem aderir às superfícies e formar estruturas resistentes que dificultam a remoção completa da contaminação. Já em situações relacionadas ao hantavírus, a preocupação está principalmente na presença de resíduos contaminados e na dispersão inadequada dessas partículas no ambiente. Em ambos os cenários, a ausência de protocolos corretos de limpeza e desinfecção pode aumentar os riscos microbiológicos e comprometer a segurança dos ambientes.
Outro ponto importante é que procedimentos incorretos de limpeza também podem representar um problema. Em locais com sinais de infestação de roedores, por exemplo, recomenda-se evitar varrer poeira seca ou utilizar métodos que levantem partículas no ar sem o devido controle, justamente para reduzir a dispersão de contaminantes. Isso reforça como a limpeza profissional vai além da remoção visual da sujeira e exige técnicas, produtos e processos adequados para minimizar riscos biológicos.
Esse cenário evidencia a importância da higienização preventiva e do controle microbiológico em empresas, hospitais, indústrias, cozinhas profissionais, condomínios e demais ambientes coletivos. Protocolos bem estruturados ajudam a reduzir contaminações invisíveis, controlar a proliferação de micro-organismos e promover ambientes mais seguros, saudáveis e preparados para prevenir riscos ambientais.
O hantavírus é transmitido pelo contato com fezes, urina e secreções de roedores infectados.
6 erros comuns na limpeza que favorecem a formação de micro-organismos
O biofilme não aparece apenas quando a limpeza é deixada de lado. Ele também pode se desenvolver quando o processo é feito de forma incompleta ou com falhas na execução. Mesmo com rotina definida e produtos adequados, pequenos erros já são suficientes para que essa estrutura se forme e continue ativa.
A seguir, veja os principais erros que podem comprometer a eficácia da limpeza e favorecer a formação de biofilmes:
1. Limpeza apenas visual
Um erro bastante comum é avaliar a limpeza apenas pela aparência da superfície. Embora isso ajude a identificar sujeira visível, não garante que o ambiente esteja realmente livre de micro-organismos.
O biofilme, principalmente nas fases iniciais, não tem cheiro, não muda a cor da superfície e não é visível a olho nu. Ou seja, uma área pode parecer limpa, mas ainda abrigar micro-organismos ativos. Usar apenas o visual como critério pode levar a uma falsa sensação de segurança.
2. Ausência de ação mecânica adequada
A fricção é uma etapa indispensável na limpeza. É ela que ajuda a romper a estrutura do biofilme e a remover as bactérias que estão aderidas à superfície.
Quando o desinfetante é aplicado sem essa ação prévia, ele tende a agir apenas nas camadas mais externas. As partes mais protegidas permanecem intactas, o que compromete o resultado. Esse erro é especialmente crítico em superfícies com irregularidades, frestas ou texturas que dificultam o contato do produto com toda a área a ser tratada.
3. Diluição incorreta de produtos
Utilizar produtos fora da concentração recomendada compromete todo o processo. Quando a diluição está abaixo da concentração mínima, o produto pode não ter força suficiente para eliminar os micro-organismos e ainda favorecer a permanência dos mais resistentes.
Por outro lado, concentrações acima do necessário não trazem ganho real de eficiência, podendo gerar resíduos indesejados e até danificar superfícies. Seguir a diluição correta é essencial para garantir equilíbrio entre desempenho e segurança.
4. Tempo de contato insuficiente do desinfetante
Todo desinfetante precisa de um tempo mínimo de ação para funcionar corretamente. Esse tempo é definido por estudos laboratoriais e especificado pelo fabricante para cada aplicação, e deve ser respeitado no uso diário.
Quando o produto é removido antes do tempo, seja por enxágue ou secagem antecipada, o processo é interrompido antes de atingir o resultado esperado. Em superfícies com biofilme, essa atenção precisa ser ainda maior, já que a ação do produto tende a ser mais lenta.
5. Ausência de protocolos padronizados
Quando não existe um padrão claro de execução, cada pessoa realiza a limpeza de uma forma diferente. Isso gera variações no resultado e dificulta o controle do processo.
Sem uma sequência definida, sem parâmetros de diluição e tempo de contato e sem critérios de avaliação, fica difícil identificar falhas e garantir consistência. Essa falta de padronização abre espaço para que o biofilme se desenvolva, especialmente em áreas que não recebem atenção constante.
6. Intervalos longos entre ciclos de higienização
O biofilme se forma de maneira contínua. Estudos demonstram que, em condições favoráveis, as primeiras etapas podem acontecer em poucas horas, e estruturas mais resistentes podem surgir em poucos dias.
Quando há muito tempo entre uma limpeza e outra, o biofilme avança para estágios mais difíceis de remover. Por isso, a frequência de higienização deve considerar o nível de risco da superfície, o fluxo de pessoas e a presença de resíduos orgânicos, e não apenas o aspecto visual.

Erros comuns na limpeza que favorecem a formação do biofilme
+SAIBA MAIS: Optizyme Detergente Enzimático
Como remover micro-organismos com detergente e ação mecânica
Quando cada etapa da limpeza é bem compreendida, o processo deixa de ser apenas uma rotina e passa a gerar resultados mais consistentes no controle microbiológico. Nesse cenário, dois pontos fazem muita diferença: o uso correto dos detergentes (incluindo limpadores desinfetantes) e a aplicação adequada da ação mecânica.
Cada um desses elementos tem uma função própria. Quando algum deles é negligenciado ou tratado como opcional, o resultado final fica comprometido.
O papel dos detergentes
Os detergentes entram antes da desinfecção e têm a função de preparar a superfície. Eles atuam sobre gorduras, proteínas e outros resíduos presentes na estrutura do biofilme, ajudando a desorganizar essa camada e facilitando o acesso do desinfetante às bactérias.
Sem essa etapa, o desinfetante encontra uma barreira que dificulta sua penetração, reduzindo sua eficiência.
A escolha do detergente deve levar em conta o tipo de sujeira e o ambiente. Produtos alcalinos são mais indicados quando há acúmulo de resíduos pesados, como gorduras e proteínas, comuns em cozinhas industriais. Já os enzimáticos atuam diretamente na quebra de componentes do biofilme, sendo mais adequados para superfícies com contaminação biológica mais complexa, como instrumentos médicos.
Os detergentes neutros são mais utilizados na limpeza de manutenção, em superfícies com menor carga orgânica.
Independentemente do tipo, é fundamental respeitar a diluição correta e o tempo de contato recomendado. Esses fatores garantem que o produto atue de forma completa. O enxágue também não deve ser negligenciado, já que resíduos podem interferir na ação do desinfetante aplicado na sequência.
“sempre que possível, considere a implementação de limpadores desinfetantes que favorecem a maior adesão ao uso dos processos de limpeza, evitando assim a formação do biofilme ou mesmo contribuindo para a sua remoção” – Luis Fernando Alves, especialista em Saneantes profissionais.
O papel da ação mecânica
A ação mecânica é indispensável. Nenhum produto químico consegue substituir completamente essa etapa. Enquanto o detergente atua na parte química, a fricção é o que rompe fisicamente a estrutura do biofilme e ajuda a remover as bactérias da superfície.
Sem esse movimento, mesmo produtos bem aplicados podem não alcançar as camadas mais protegidas, permitindo que o biofilme continue presente.
A forma de aplicar essa ação deve considerar o tipo de superfície e o nível de contaminação. Em áreas lisas, a fricção com pano ou escova costuma ser suficiente, desde que feita com pressão e cobertura adequadas. Já em equipamentos com frestas, cantos ou formatos mais complexos, pode ser necessário utilizar escovas específicas, jatos de alta pressão ou até lavadoras ultrassônicas, garantindo que todas as áreas sejam alcançadas.
Por que os desinfetantes nem sempre controlam a contaminação nas superfícies
Os desinfetantes costumam ser vistos como o principal recurso no controle microbiológico. No entanto, o resultado que eles entregam depende diretamente de tudo o que foi feito antes. Quando as etapas anteriores não são bem executadas, o desempenho do desinfetante tende a cair.
De forma geral, esses produtos atuam destruindo a estrutura das células, afetando proteínas essenciais e interferindo em processos internos importantes para a sobrevivência dos micro-organismos. Para que isso funcione, é necessário que o produto chegue até essas células na concentração correta e permaneça em contato pelo tempo adequado.
No caso do biofilme, isso se torna mais difícil. Pois a EPS (estrutura que envolve os micro-organismos funciona como uma barreira), retarda a ação do desinfetante e, em alguns casos, reduzindo parte do seu efeito antes mesmo que ele alcance as camadas mais internas.
Para melhorar o desempenho nesse cenário, alguns pontos precisam ser bem controlados:
Tipo de princípio ativo
Nem todo desinfetante reage da mesma forma diante do biofilme. A escolha do produto deve considerar sua capacidade de penetrar nessa estrutura e sua indicação para o tipo de superfície e micro-organismo envolvido, sempre com base em critérios técnicos e conformidade com a ANVISA.
Concentração
Manter a diluição correta é indispensável. Quando o produto é utilizado abaixo do recomendado, o resultado pode ser insuficiente e ainda favorecer a permanência de micro-organismos mais resistentes.
Tempo de contato
O produto precisa permanecer na superfície pelo tempo indicado para agir corretamente. Como a penetração no biofilme é mais lenta, esse cuidado se torna ainda mais importante.
Limpeza prévia
A remoção de resíduos antes da desinfecção faz toda a diferença. Sem essa etapa, o desinfetante pode ser bloqueado antes de atingir os micro-organismos, reduzindo sua eficácia.
Nenhum desinfetante, isoladamente, resolve o problema de um biofilme já formado. O resultado depende da qualidade do processo como um todo, desde a limpeza inicial até a aplicação correta dos produtos.
Como prevenir e controlar o biofilme na rotina de limpeza
Controlar o biofilme exige mais do que uma rotina de limpeza. É preciso ter consistência, critérios claros e um processo bem organizado. Frequência de higienização, escolha de produtos, preparo da equipe e acompanhamento dos resultados precisam caminhar juntos. Quando esses pontos não estão alinhados, o controle perde eficiência.
Frequência adequada de higienização
A frequência de limpeza ainda é um ponto que costuma ser subestimado. Definir intervalos apenas com base no que é visível não é suficiente para evitar o avanço do biofilme.
O ideal é que a frequência seja ajustada de acordo com o risco de cada superfície e revisada sempre que necessário, considerando o histórico do ambiente.
Como referência geral:
- Superfícies críticas (contato direto com pacientes ou alimentos): limpeza a cada uso ou, no mínimo, a cada turno;
- Superfícies semicríticas (equipamentos de apoio e contato indireto): limpeza diária ou conforme protocolo;
- Superfícies de menor risco (áreas administrativas e corredores): frequência ajustada ao fluxo de pessoas e às características do local.
Independentemente dessa classificação, qualquer superfície visivelmente contaminada deve ser higienizada imediatamente.
Produtos com ação oxidante podem auxiliar na quebra da estrutura microbiológica do biofilme, favorecendo a eliminação de microrganismos aderidos às superfícies.
Além disso, utilizar produtos adequados para esse tipo de desafio ajuda a dar mais consistência ao processo. A Hygibras trabalha com soluções desenvolvidas para diferentes níveis de sujidade e criticidade, o que permite ajustar a limpeza conforme a necessidade de cada ambiente.
Na prática, isso facilita a escolha do produto certo para cada etapa, seja na remoção de resíduos, na quebra da estrutura do biofilme ou na desinfecção. Essa combinação torna o processo mais eficiente e reduz a chance de falhas que passam despercebidas no dia a dia.
Outro ponto importante é que produtos bem formulados também contribuem para padronizar a rotina, tornando a aplicação mais simples para a equipe e mantendo o resultado mais estável ao longo do tempo.
+SAIBA MAIS: Desinfetante e Detergente Garra Oxiativo Pronto Uso
Treinamento das equipes de higienização
A execução correta dos processos de higienização depende do nível de compreensão técnica dos profissionais envolvidos. Quando os profissionais não entendem como o biofilme se forma e se comporta, erros tendem a se repetir, mesmo com rotinas já definidas.
Por isso, o treinamento precisa ir além do “como fazer” e incluir o entendimento do problema que está sendo controlado. A atualização periódica, com avaliações práticas, ajuda a manter o padrão de execução e melhora os resultados ao longo do tempo.
Em nossa empresa, conte com vários módulos de treinamentos que ampliam a adesão ao uso correto de procedimentos!

Com o treinamento Hygibras você garante uma equipe capacitada para uma limpeza ainda mais profissional.
Validação e critérios de escolha de produtos
Nem sempre um produto adequado no papel apresenta o mesmo desempenho no dia a dia. Por isso, a escolha precisa considerar o tipo de micro-organismo, o material da superfície e os resultados obtidos no próprio ambiente.
Laudos técnicos e estudos com resultados comprovados ajudam a embasar essa decisão e devem ser considerados antes de qualquer mudança ou padronização.
Monitoramento microbiológico
Acompanhar os resultados é o que mostra se as práticas adotadas estão funcionando. Existem diferentes formas de fazer isso. A bioluminescência por ATP permite identificar rapidamente a presença de matéria orgânica e micro-organismos.
Já métodos como swabs e placas de contato trazem dados comparáveis ao longo do tempo. Indicadores químicos e biológicos também são utilizados em processos mais críticos, como esterilização.
Registrar e analisar esses dados com frequência permite identificar pontos de atenção antes que se tornem problemas maiores. Esse acompanhamento contínuo ajuda a ajustar o processo e manter o controle ao longo do tempo.
“Uma opção bastante conveniente é o uso do sistema de monitoramento Optiglow, pois com muita facilidade a gestão consegue analisar se procedimentos estão ocorrendo de forma adequada, antes de aprofundamentos mais onerosos e demorados que a validação por ATP, por exemplo.”
Opinião de um especialista sobre essa contaminação microbiológica
Paulo Henrique Weckwerth, professor e pesquisador, doutor em Doenças Tropicais pela UNESP e pós-doutor em Microbiologia pela Faculdade de Odontologia de Bauru da USP. Atua há mais de 27 anos no ensino e na pesquisa em Microbiologia Clínica, Microbiologia Oral e Resistência Bacteriana.
“Os biofilmes microbianos são um dos maiores desafios para a higiene hospitalar e de muitos outros ambientes porque transformam micro-organismos comuns em comunidades altamente protegidas e resilientes, podendo ser até 1.000 vezes mais resistentes a antibióticos e desinfetantes do que bactérias em estado planctônico. Superfícies visualmente limpas podem abrigar biofilmes maduros, falhando no controle de infecções e servindo como fonte de contaminação cruzada.
Além disso, a troca de informações genéticas entre os componentes do biofilme representa um problema adicional de grande relevância, pois acelera a disseminação de mecanismos de resistência entre as células da comunidade. Por isso, o biofilme é frequentemente subestimado: não é visível a olho nu e se forma em dispositivos hospitalares por bactérias de elevado grau de patogenicidade, como Staphylococcus aureus e Pseudomonas aeruginosa.
Seu controle exige métodos de higienização avançados, com ação mecânica efetiva e produtos adequados, a fim de garantir a segurança dos pacientes e de todos os profissionais envolvidos.”
Produtos de limpeza para eliminar o biofilme
A eficácia da limpeza hospitalar não depende apenas da técnica, mas também da escolha correta dos produtos utilizados em cada etapa do processo.
Em ambientes assistenciais, onde a carga microbiológica é elevada e a presença de matéria orgânica é frequente, o uso de soluções inadequadas pode comprometer diretamente o resultado da higienização.
Oxikil Pronto Uso
Uma alternativa prática e eficiente para a desinfecção de superfícies, indicada para rotinas que exigem rapidez sem comprometer o desempenho.
Sua formulação pronta para uso permite aplicação direta, sem necessidade de diluição, o que ajuda a reduzir erros operacionais e manter maior padronização no processo. É recomendado para superfícies de alto contato, auxiliando na redução da carga microbiana em pontos críticos e contribuindo para o controle de micro-organismos associados à formação de biofilme em ambientes hospitalares.
+SAIBA MAIS: Desinfetante Hospitalar Optigerm Oxikill Pronto Uso
Optizyme
Atua na etapa de limpeza como um detergente enzimático, desenvolvido para remover matéria orgânica como sangue, secreções e outros resíduos biológicos.
Sua ação contribui para a quebra dessas sujidades, favorecendo uma limpeza mais eficiente e preparando a superfície para a etapa de desinfecção. Esse tipo de produto é importante em cenários onde a presença de matéria orgânica pode proteger micro-organismos e favorecer a formação de biofilme, dificultando a ação dos desinfetantes.
+SAIBA MAIS: Optizyme Detergente Enzimático
Garra Oxiativo Pronto Uso
Atua na etapa de limpeza e desinfecção, sendo um detergente bactericida à base de peróxido ativado, indicado para a remoção de sujidades em superfícies laváveis.
Sua ação reage com a matéria orgânica, formando pequenas bolhas efervescentes que auxiliam na remoção da sujeira, permitindo uma limpeza mais eficiente e reduzindo a necessidade de ação mecânica mais intensa. Esse tipo de produto contribui para melhorar o desempenho da limpeza, especialmente em áreas com maior acúmulo de resíduos.
Em cenários onde a presença de matéria orgânica pode favorecer a formação de biofilme, essa etapa é importante para reduzir interferências e facilitar a ação dos desinfetantes aplicados na sequência.
+SAIBA MAIS: Desinfetante e Detergente Garra Oxiativo Pronto Uso
FAQ: Perguntas frequentes sobre biofilmes
O que são biofilmes?
Biofilmes são grupos de micro-organismos que se fixam em superfícies e formam uma camada protetora ao redor das células. Essa estrutura aumenta a resistência aos desinfetantes e outros agentes químicos, o que dificulta a eliminação. Eles são comuns em ambientes hospitalares, industriais e alimentícios, onde representam um desafio constante para o controle microbiológico.
O que é biofilme bacteriano?
O biofilme bacteriano se forma quando bactérias se aderem a uma superfície e passam a produzir uma estrutura que as envolve e protege. Isso aumenta a capacidade de sobrevivência, inclusive diante da ação de desinfetantes e antibióticos. Espécies como Staphylococcus aureus, Pseudomonas aeruginosa e Listeria monocytogenes são exemplos relevantes, frequentemente associadas a infecções hospitalares e contaminações em ambientes de produção de alimentos.
Como os biofilmes se formam nas superfícies?
A formação do biofilme acontece em etapas. Primeiro, as bactérias se aproximam e se fixam de forma leve. Depois, essa fixação se torna mais firme, iniciando a produção da camada protetora. Em seguida, ocorre a multiplicação e formação de pequenas colônias, até que a estrutura amadurece e se torna mais resistente. Por fim, parte dessas bactérias se desprende e pode colonizar novas superfícies. Em condições favoráveis, esse processo pode começar em poucas horas.
Por que biofilmes são difíceis de remover?
A dificuldade está na combinação de vários fatores. A camada protetora dificulta a entrada dos desinfetantes, as bactérias mais internas reduzem sua atividade para resistir, a estrutura não é uniforme e algumas células ainda produzem substâncias que neutralizam os produtos químicos. Tudo isso torna o biofilme mais resistente do que bactérias livres.
Biofilmes podem causar contaminação?
Sim. O biofilme libera micro-organismos continuamente para o ambiente, o que facilita a contaminação entre superfícies, equipamentos, alimentos e pessoas. Estudos indicam que muitas infecções têm relação com a presença de biofilmes, o que mostra o impacto direto na segurança sanitária.
Como eliminar biofilme em superfícies?
A remoção do biofilme exige um processo completo. É necessário remover os resíduos visíveis, aplicar o detergente adequado com ação mecânica, enxaguar, aplicar o desinfetante na concentração correta e respeitar o tempo de contato indicado. Quando necessário, deve-se realizar o enxágue final. Nenhuma dessas etapas substitui a outra. A regularidade do processo, a escolha dos produtos e o preparo da equipe fazem toda a diferença no resultado.
Hygibras: sua aliada no controle do biofilme
Ao longo deste artigo, você viu que o biofilme é um problema microbiológico, persistente e com consequências concretas para a segurança sanitária. Em estabelecimentos de saúde, contribui para o aumento das taxas de infecção, prolonga internações e intensifica o uso de antimicrobianos. Na indústria alimentícia, coloca em risco a segurança dos produtos e a integridade das operações.
Também ficou claro que esse tipo de contaminação vai além do alcance dos métodos convencionais de higienização. O biofilme pode permanecer ativo mesmo em superfícies aparentemente limpas, exigindo uma abordagem mais técnica e consistente.
O próximo passo é avaliar como esse controle acontece hoje na sua rotina. A limpeza está baseada apenas no que é visível? As etapas estão sendo seguidas corretamente? Existe um padrão claro de execução? Esses pontos ajudam a identificar onde o biofilme pode estar se desenvolvendo sem ser percebido.
Controlar esse problema exige uma mudança de postura. Mais do que limpar, é preciso adotar uma abordagem preventiva, baseada no entendimento de como o biofilme se forma, como resiste e em quais condições se desenvolve. Sem isso, mesmo processos bem estruturados e produtos adequados podem não ser suficientes.
Quando essa visão passa a fazer parte da rotina, a higienização ganha outro nível de importância. Deixa de ser apenas uma atividade operacional e passa a contribuir diretamente para a segurança, a continuidade das operações e a manutenção de um padrão confiável ao longo do tempo.
Ou, se preferir, acesse nossos materiais gratuitos e aprimore sua gestão de higiene profissional com base técnica:
✅Conheça a Cronograma de Limpeza da Hygibras
✅Calculadora de Diluição de Produtos de Limpeza
✅Saiba tudo sobre a Limpeza por Cores
Esclarecer dúvidas, orientar e oferecer sempre o melhor em técnicas e produtos de limpeza profissional é a nossa missão na Hygibras. Conte sempre com a gente para fazer escolhas que atendam às necessidades de sua empresa.
Se você gostou de entender um pouco mais sobre biofilme, compartilhe com mais pessoas, nos acompanhe nas redes sociais, nos siga nas plataformas de áudio e acompanhe nosso site para não perder dicas de limpeza profissional e conhecer nossas soluções de limpeza profissional.
Até o próximo!
Referências: